Cerium
Cerium • Ce • Ordnungszahl 58

Cerium
Cer ist ein silbergraues, relativ weiches, duktiles, paramagnetisches und reaktives Metall. Es ist das am häufigsten vorkommende Lanthanoid und ist in etwa so häufig wie Kupfer. Es gehört zu den leichten Seltenen Erden.
1803 entdeckten der schwedische Chemiker Jöns Jacob Berzelius zusammen mit Wilhelm Hisinger das Element. Unabhängig davon entdeckte es zeitgleich auch der deutsche Chemiker Martin Klaproth. Es wurde nach dem kurz zuvor entdeckten Zwergplaneten Ceres benannt.
Wie die meisten der Seltenerdelemente wurde auch dieses zunächst in Form seines Oxids, des sogenannten Ceriumdioxid (Cer(IV)oxid), identifiziert und erst Jahrzehnte nach seiner Entdeckung als reines Metall gewonnen.
In der 2. Hälfte des 19. Jahrhunderts entwickelte Carl Auer von Welsbach mit großem Erfolg zwei Produkte, die den Einsatz von Cer erfordern: Gashüllen und Feuersteine (Zündstein). Auers Gashüllen ermöglichten ein helles, weisses Licht in Gaslampen.
Wie andere Elemente der Seltenen Erden ist Cer in der Natur nie in seiner reinen Form zu finden. Es wird aus Mineralien wie Xenotim, Monazit und Bastnäsit oder aus Ionen-Adsorptionstonen gewonnen.

-
Vorkommen
Cer wird hauptsächlich aus cerhaltigem Monazit und Bastnäsit gewonnen. Es kommt auch in Allanit, Zerit, Samarskit und dem Titanmineral Perowskit vor. Es wird in den USA, China, Russland, Australien und Indien abgebaut.
In der Natur kommen vier stabile bzw. besonders langlebige Isotope vor: stabiles Cer-140 (88,48 Prozent) und radioaktives Cer-142 (11,08 Prozent), Cer-138 (0,25 Prozent) und Cer-136 (0,19 Prozent). Ohne die Kernisomeren wurden insgesamt 38 radioaktive Isotope von Cer charakterisiert. Sie liegen in der Masse zwischen 119 und 157 mit Halbwertszeiten von nur 1,02 Sekunden für Cer-151 und 5 × 1016 Jahren für Cer-142.

Cer-oxid -
Gewinnung
Das Metall wird durch Elektrolyse und metallothermische Reduktion der Halogenide mit Alkali- oder Erdalkalimetallen hergestellt. Es existiert in vier allotropen (strukturellen) Formen. Die α-Phase ist flächenzentriert kubisch (FCC) mit a = 4,85 Å bei 77 K (-196 °C, oder -321 °F). Die β-Phase bildet sich knapp unter Raumtemperatur und ist doppelt dicht gepackt hexagonal (DHCP) mit a = 3.6810 Å und c = 11.857 Å. Die γ-Phase ist die Raumtemperaturform und ist kubisch flächenzentriert (FCC) mit a = 5.1610 Å bei 24 °C (75 °F). Die δ-Phase ist kubisch-körperzentriert (BCC) mit a = 4,12 Å bei 757 °C (1.395 °F).
Nach einer aufwendigen Abtrennung der Cer-Begleiter wird das Oxid mit Fluorwasserstoff zum Cerfluorid umgesetzt. Anschließend wird es mit Calcium unter Bildung von Calciumfluorid zum Cer reduziert. Die Abtrennung verbleibender Calciumreste und Verunreinigungen erfolgt in einer zusätzlichen Umschmelzung im Vakuum.
-
Verwendung
Obwohl Seltene Erden als kritische Rohstoffe eingestuft werden, trifft Knappheit nicht auf alle Seltenerdelemente zu. Wie bereits erwähnt ist Cer das häufigste unter den Seltenen Erden. Da die Seltenen Erden in Lagerstätten stets zusammen vorkommen und abgebaut werden, führt dies bei Cer (und Lanthan, dem zweithäufigsten Seltenerdelement) zu einer erheblichen und anhaltenden Überproduktion.
Trotz Nachfrage nach Cer und Lanthan, ist diese bei weitem nicht groß genug, um das massive Angebot aufzunehmen, das durch den Abbau anfällt.
Seine Fähigkeit, zwischen den Oxidationsstufen Ce³⁺ und Ce⁴⁺ zu wechseln, macht es besonders nützlich in katalytischen und redoxaktiven Prozessen. Die größte Anwendung für Cer ist etwa in Auto-Abgaskatalysatoren. In Drei-Wege-Katalysatoren ist Ceroxid eine entscheidende Komponente. Ein weiterer großer Anwendungsbereich ist in Fluid Catalytic Cracking(FCC)-Katalysatoren in Ölraffinerien.
Ceroxid (CeO₂) ist außerdem ein hervorragendes Poliermittel für Glas, Linsen und Siliziumwafern.
In der Glas- und Keramikindustrie wird Cer Glas und Glasuren als Zusatzstoff beigemischt, um bestimmte Eigenschaften zu erreichen. Etwa zum Entfärben durch die Beseitigung von Verunreinigungen im Glas und Keramikglasuren. Dadurch wird Glas klarer und Keramikglasur reiner. Cer kann Glas auch eine gelbe Färbung verleihen, die als Schutz vor UV-Strahlung genutzt wird.
Cer wird auch weiterhin für Beleuchtungen genutzt. In Energiesparlampen verbessert Cer in Leuchtstoffphosphoren die Lichtqualität. In weißen LEDs sind Cer-dotierte Leuchtstoffe (z.B. YAG:Ce) die Schlüsselkomponente.
In kleinen Mengen Aluminium- oder Magnesiumlegierungen zugesetzt, verbessert es deren Korrosionsbeständigkeit und mechanische Eigenschaften.
Cerhaltige Beschichtungen und Konversionsschichten (z.B. auf Aluminium oder Stahl) bieten einen hervorragenden Schutz gegen Korrosion und werden als umweltfreundlichere Alternative zu chromathaltigen Beschichtungen erforscht.
Cerdioxid-basierte Materialien werden in Festoxid-Brennstoffzellen als Elektrolyt verwendet, da sie Ionen leitfähig sind.
Cer-reiche Legierungen (z.B. mit Kobalt oder Eisen) können Wasserstoff absorbieren und wieder abgeben und sind Gegenstand der Forschung für Speichertechnologien.
Cer wird auch heute noch für den Zündstein in Feuerzeugen verwendet, eine der ersten kommerziellen Anwendungen des Elements im 19. Jahrhundert, eingeführt vom geschäftstüchtigen Chemiker Carl Auer von Welsbach.
-
Besonderheiten
Das silbrigweiß glänzende Metall ist hinter Europium das zweitreaktivste Element der Lanthanide. Oberflächliche Verletzungen der schützenden gelben Oxidschicht entzünden das Metall. Oberhalb von 150 °C verbrennt es unter heftigem Glühen zum Cerdioxid. Mit Wasser reagiert es zum Cerhydroxid.
Cer kommt in Verbindungen als dreiwertiges, farbloses oder vierwertiges, gelbes bis orangefarbenes Kation vor.
Unter Wärmeeinfluss wird es durch Ethanol und Wasser sehr stark angegriffen. Auch in Laugen wird es unter Bildung von Cer-Hydroxiden stark angegriffen. In Säuren wird es zu Salzen gelöst. Da sich die chemischen Eigenschaften der Seltenen Erden ähneln, wird metallisches Cer selten in Reinform eingesetzt, sondern in der Mischung, in der es bei der Herstellung aus den Seltenerd-Mineralien anfällt, dem sogenannten Mischmetall.
Cer ist, wie alle Lanthanoide, leicht giftig. Metallisches Cer kann sich schon ab 65 °C entzünden. Als fein verteiltes Metall kann es sich an der Luft ohne Energiezufuhr erhitzen und schließlich entzünden. Die Zündbereitschaft hängt u. a. sehr stark von der Korngröße und dem Verteilungsgrad ab. Cerbrände dürfen nicht mit Wasser gelöscht werden, da sich dabei explosives Wasserstoffgas entwickeln würde.
Cer unterscheidet sich neben Praseodym und Terbium von den anderen Seltenen Erden dadurch, dass es Verbindungen bildet, in denen seine Oxidationsstufe +4 ist. In Lösungen ist es sogar die einzige Seltene Erde, die eine +4 Oxidationsstufe aufweist. Salze des Ce4+-Ions (Kernsalze), die leistungsfähige, aber stabile Oxidationsmittel sind, werden in der analytischen Chemie verwendet, um oxidierbare Substanzen wie Eisen (Eisen in der Oxidationszone +2) zu bestimmen. Cer in seinem Oxidationszustand von +3 verhält sich wie eine typische Seltene Erde.
Allgemein Name, Symbol, Ordnungszahl Cer, CE, 58 Serie Lanthanoide Gruppe, Periode, Block La, 6, f Aussehen silbrig weiß CAS-Nummer 7440-45-1 Massenanteil an der Erdhülle 43ppm Atomar Atommasse 140,116 u Atomradius 185 pm Kovalenter Radius 204 pm Elektronenkonfiguration [Xe] 4f 1 5d 1 6s 2 1. Ionisierungsenergie 5,5386(4) eV ≈ 534 KJ/mol 2. Ionisierungsenergie 10,956(20) eV ≈ 1057 KJ/mol 3. Ionisierungsenergie 20,1974(25) eV ≈ 1949 KJ/mol 4. Ionisierungsenergie 36,906(9) eV ≈ 3561 KJ/mol 5. Ionisierungsenergie 65,55(25) eV ≈ 6320 kJ/mol Physikalisch Aggregatszustand fest Kristallstruktur kubisch flächenzentriert Dichte 6,773 g/cm3 (25 °C) Mohshärte 2,5 Magnetismus paramagnetisch (χm = 1,4 * 10−3) Schmelzpunkt 1068 K (795 °C) Siedepunkt 3743 K (3470 °C) Molares Volumen 20,69 * 10-6 m3/mol Verdampfungswärme 398 KJ/mol Schmelzwärme 5,5 KJ/mol Schallgeschwindigkeit 2100 m/s bei 293,15 K Elektrische Leitfähigkeit 1,35 * 106 S/m Wärmeleitfähigkeit 11 W/(m*K)

- Aufrufe: 4468

 = 7,8 · 10−5)
= 7,8 · 10−5)


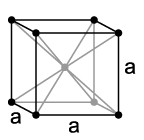
 und dem Gitterparameter a = 302,4 pm sowie zwei Formeleinheiten pro Elementarzelle.
und dem Gitterparameter a = 302,4 pm sowie zwei Formeleinheiten pro Elementarzelle.