Wolfram
W • Ordnungszahl 74
Wolfram
Wolfram ist ein weißglänzendes außergewöhnlich hartes, sehr dichtes und seltenes Metall mit einer guten elektrischen Leitfähigkeit. Es hat mit 3.422 Grad Celsius den höchsten Schmelzpunkt unter allen chemischen Elementen.
Seine bekannteste Verwendung ist die als Glühdraht in Glühbirnen
Die wichtigste Anwendung ist als Legierungszusatz in Stählen, um Härte und Festigkeit in Industriewerkzeugen zu erhöhen, sowie als Wolframcarbid in Industriewerkzeugen und militärischen Anwendungen.
China ist mit Abstand der größte W-Produzent und repräsentiert über 83 % der weltweiten Produktion.
Die Xihuashan Mine in China ist die größte aktive Wolfram-Mine der Welt. Sie wird von China Tungsten High-Tech betrieben.
Aufgrund seiner Seltenheit und Anwendung im militärischen Bereich gilt Tungsten als kritischer Rohstoff in der EU, den USA, Japan, Südkorea, Großbritannien, Australien und Kanada.
-
Geschichte
1781 hatte der schwedische Chemiker Carl Wilhelm Scheele Wolframsäure in einem Mineral entdeckt, das heute als Scheelit bekannt ist. Sein Landsmann Torbern Bergman folgerte, dass aus der Säure ein neues Metall hergestellt werden könne.
Dies gelang den Brüdern und Chemikern Juan José und Fausto Elhuyar 1783 durch Holzkohlereduktion von Wolframit aus dem sächsischen Erzgebirge.Der Name Wolfram geht auf den Freiberger Mineralogen Georgius Agricola zurück, der wahrscheinlich schon im 16. Jahrhundert ein wolframhaltiges Mineral beschrieb und den lateinischen Namen„lupi spuma“ gab, was Wolfsschaum bedeutet. Die in anderen Sprachen gebräuchliche Bezeichnung „tungsten“ kommt aus dem Schwedischen und bedeutet „schwerer Stein“.
Wegen seiner extrem hohen Schmelztemperatur war Wolfram zunächst schwer zu verarbeiten.
Ab Mitte des 19. Jahrhundert wurde Wolfram in Stahllegierungen verwendet, um härtere Werkzeuge herzustellen.
Ende des 19. Jahrhunderts mit dem Aufkommen von elektrischem Licht ersetzte Wolframdraht, der es nicht so schnell schmolz, die Kohlefäden in Glühbirnen.
Im 20. Jahrhundert wurde Wolframcarbid (WC) wird für panzerbrechende Munition und extrem harte Schneidwerkzeuge entwickelt.
-
Verwendung
Aufgrund seiner außergewöhnlichen physikalischen Eigenschaften wird Wolfram für eine Vielzahl von Anwendungen eingesetzt. Wolframcarbid wird für die Herstellung von Hartmetallen für Schneid-, Bergbau und Drahtziehwerkzeugen, verwendet sowie auch in der Rüstungsindustrie für panzerbrechende Munition, in Granaten und für Panzerungen.
In Legierungen sorgt Wolfram für Hitzebeständigkeit in Ventilen, Turbinenrädern von Flugzeugtriebwerken und Raketendüsen und schützt gleichzeitig vor Verschleiß.
Wolfram wird auch in der Elektronik in Elektroden, der Halbleiterindustrie für Mikrochips und in Röntgenröhren verwendet.
Wegen seiner Dichte wird Wolfram auch für Strahlenabschirmung genutzt.
-
Vorkommen, Abbau, Gewinnung
Zu den wichtigen Erzen zählen Wolframit und Scheelit.
Über 80 Prozent des Wolframs werden in China gefördert, das auch über einige der größten Wolfram-Vorkommen verfügt. Die Xihuashan-Mine in der Provinz Jiangxi, ist die größte aktive Wolframmine der Welt. Sie wird betrieben von Tungsten High-Tech, ein Tochterunternehmen der staatlichen China Minmetals Corporation.
Nach China ist Vietnam das zweitgrößte Abbauland für Wolfram. Die Nui Phao Mine in Vietnam ist die größte Wolframmine außerhalb Chinas. Der Betreiber ist Masan Resources. Russland steht an dritter Stelle, Zahlen zu Fördermengen sind jedoch rar.
In der EU gibt es auch einige Wolframproduzente. In Österreich betreibt die Wolfram Bergbau und Hütten AG einen kleinen Untertagebau in den Alpen. Den Großteil des Rohstoffs gewinnt das Unternehmen, das zur schwedischen Sandvik-Gruppe gehört, aus Recycling. Daneben sind Portugal und Spanien kleinere Wolframminen in Betrieb.
Die globale Jahresproduktion beläuft sich auf etwa 80.000 Tonnen.
Die Wiederverwertung von Schrotten ist, eine wichtige Quelle für die Wolframindustrie.
-
Substitution
Mögliche Ersatzstoffe für Wolframkarbide sind Hartmetalle auf Basis von Molybdänkarbid, Niobkarbid oder Titankarbid, Keramik, keramisch-metallische Verbundwerkstoffe und Werkzeugstähle. Die meisten dieser Optionen reduzieren den Wolframverbrauch, anstatt ihn zu ersetzen.
Mögliche Ersatzstoffe für andere Anwendungen sind: Molybdän für bestimmte Wolframwalzprodukte; Molybdänstähle für Wolframstähle, obwohl die meisten Molybdänstähle weiterhin Wolfram enthalten.
Abgereichertes Uran oder Blei ersetzen Wolfram oder Wolframlegierungen in Anwendungen, die eine hohe Dichte oder die Fähigkeit zur Strahlungsabschirmung erfordern.
Abgereicherte Uranlegierungen oder gehärteter Stahl kann Wolframkarbide oder Wolframlegierungen in panzerbrechenden Geschossen substituieren.
In manchen Anwendungen würde ein Ersatz zu höheren Kosten oder einer Beeinträchtigung der Leistung führen. -
Eigenschaften
Physikalische Eigenschaften
Wolfram ist ein weißglänzendes, in reinem Zustand dehnbares Metall hoher Härte, Dichte und Festigkeit. Die Dichte ist fast gleich hoch wie die von Gold, die Brinellhärte beträgt 250 HB, die Zugfestigkeit 550-620 N/mm2 (weich) bis 1920 N/mm2 (hart). Das Metall existiert in einer stabilen kubisch-raumzentrierten α-Modifikation mit einem Netzebenenabstand (=Gitterkonstante) von 316 pm bei Raumtemperatur. Dieser Kristallstrukturtyp wird häufig Wolfram-Typ genannt. Bei einer als metastabile β-Modifikation des Wolframs (verzerrt kubisch-raumzentriert) bezeichneten Substanz handelt es sich hingegen um das wolframreiche Oxid W3O.
Wolfram besitzt nach dem Element Kohlenstoff mit 3422 °C den zweithöchsten Schmelzpunkt aller chemischen Elemente. Der Siedepunkt von 5555 °C wird nur noch von dem seltenen Metall Rhenium mit 5596 °C um 41 K übertroffen.
Das Metall ist ein Supraleiter mit einer Sprungtemperatur von 15 mK.
Chemische Eigenschaften
Wolfram ist ein chemisch sehr widerstandsfähiges Metall, das selbst von Fluorwasserstoffsäure und Königswasser (zumindest bei Zimmertemperatur) kaum angegriffen wird. Es löst sich aber in Gemischen aus Fluss- und Salpetersäure und geschmolzenen Gemischen aus Alkalinitraten und -karbonaten auf.
-
Isotope
Von Wolfram sind 33 Isotope und 5 Kernisomere bekannt. In der Natur kommen davon 5 Isotope vor 180W, 182W, 183W, 184W und 186W. Das Wolframisotop 184W weist dabei die größte Häufigkeit auf. Alle 5 natürlichen Isotope wurden lange Zeit für stabil gehalten. Erst 2004 gelang dem CRESST Experiment am Laboratori nazionali del Gran Sasso als Nebenergebnis der Suche nach Dunkler Materie der Nachweis, dass das Isotop 180W dem Alphazerfallunterliegt. Die Halbwertszeit beträgt extrem lange 1,8 Trillionen Jahre, daher ist dieser Zerfall in normaler Laborumgebung nicht nachweisbar. Die Radioaktivität dieses natürlichen Isotops ist so gering, dass sie für alle praktischen Zwecke ignoriert werden kann. Die künstlichen radioaktiven Isotope von Wolfram haben dagegen kurze Halbwertszeiten zwischen 0,9 ms bei 185W und 121,2 Tagen bei 181W.
-
Sicherheitshinweise
Als Pulver oder Staub ist es leicht entzündlich, in kompakter Form nicht brennbar.
-
Verbindungen
Oxide
Wolfram bildet mehrere Oxide. Zwischen dem Anfangsglied:
- Wolfram(VI)-oxid WO3 – zitronengelb
und dem Endglied:
- Wolfram(IV)-oxid WO2 – braun
gibt es noch folgende intermediäre Oxide:
- W10O29 blauviolett, Homogenitätsbereich WO2,92-WO2,88
- W4O11 rotviolett, Homogenitätsbereich WO2,76-WO2,73
- W18O49, WO2,72
- W20O50, WO2,50
Sonstige Verbindungen
- Natriumwolframat Na2WO4
- Zirkoniumwolframat ZrW2O8 zeigt beim Erwärmen eine Anomalie.
- Wolframbronzen MxWO3; M=Alkali-,Erdalkalimetall,Lanthanoid, ca. 0.3 < x < 0.9 besitzen elektrische Leitfähigkeit und sind intensiv und je nach Metallgehalt unterschiedlich gefärbt.
- Calciumwolframat CaWO4 ist als Mineral unter dem Namen Scheelit bekannt.
- Wolframcarbid WC ist eine extrem harte metallähnliche Verbindung. Daneben gibt es noch Diwolframcarbid W2C.
- Wolframhexafluorid WF6
- Bleiwolframat PbWO4
- Wolframdisulfid WS2 Einsatz als trockenschmiermittel (Ähnlich MoS2)
Verwendung der Verbindungen
Wolframcarbid wird als Neutronenreflektor bei Kernwaffen eingesetzt, um die kritische Masse herabzusetzen. Wolframcarbide (Hartmetall) werden aufgrund ihrer hohen Härte in der Materialbearbeitung verwendet.
Wolframate werden zur Imprägnierung von Stoffen verwendet, um diese schwer entflammbar zu machen.
Wolframhaltige Farben werden in der Malerei sowie in der Keramik- und Porzellanindustrie verwendet.
Bleiwolframat wird als moderner Szintillator in der Teilchenphysik verwendet.
Allgemein Name, Symbol,Ordnungszahl Wolfram, W, 74 Serie Übergangsmetalle Gruppe, Periode, Block 6, 6, d Aussehen gräulich weiß, glänzend CAS-Nummer 7440-33-7 Massenanteil an derErdhülle 64 ppm Atomar Atommasse 183,84 u Atomradius (berechnet) 135 (193) pm Kovalenter Radius 162 pm Elektronenkonfiguration [Xe] 4f145d46s2 1. Ionisierungsenergie 770 kJ/mol 2. Ionisierungsenergie 1700 kJ/mol Physikalisch Aggregatzustand fest Kristallstruktur kubisch raumzentriert Dichte 19,3 g/cm3 (20 °C) Mohshärte 7,5 Magnetismus paramagnetisch (  = 7,8 · 10−5)
= 7,8 · 10−5)Schmelzpunkt 3695 K (3422 °C) Siedepunkt 5828 K (5555 °C) Molares Volumen 9,47 · 10−6 m3/mol Verdampfungswärme 824 kJ/mol Schmelzwärme 35,4 kJ/mol Schallgeschwindigkeit 5174 m/s Spezifische Wärmekapazität 138 J/(kg · K) Elektrische Leitfähigkeit 18,52 · 106 A/(V · m) Wärmeleitfähigkeit 170 W/(m · K) Chemisch Oxidationszustände 6, 5, 4, 3, 2 Normalpotential −0,119 V (WO2 + 4H+ + 4e−
→ W + 2H2O)Elektronegativität 2,36 (Pauling-Skala) Isotope Isotop NH t1/2 ZA ZE (MeV) ZP 178W {syn.} 21,6 d ε 0,091 178Ta 179W {syn.} 37,05 min ε 1,060 179Ta 180W 0,13 % 1,8 · 1018 a α 2,516 176Hf 181W {syn.} 121,2 d ε 0,188 181Ta 182W 26,3 % Stabil 183W 14,3 % Stabil 184W 30,67 % Stabil 185W {syn.} 75,1 d β− 0,433 185Re 186W 28,6 % Stabil 187W {syn.} 23,72 h β− 1,311 187Re 188W {syn.} 69,4 d β− 0,349 188Re NMR-Eigenschaften Spin γ in
rad·T−1·s−1Er(1H) fL bei
B = 4,7 T
in MHz183W 1/2 1,128 · 107 1,07 · 10−5 4,166 Sicherheitshinweise GHS-GefahrstoffkennzeichnungPulver 
GefahrH- und P-SätzeH: 228EUH: keine EUH-SätzeP: 210-240-241-280-370+378 Gefahrstoffkennzeichnung

Leicht-
entzündlich(F) PulverR- und S-SätzeR: 11S: 43

- Aufrufe: 2403


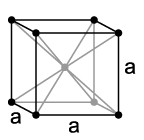
 und dem Gitterparameter a = 302,4 pm sowie zwei Formeleinheiten pro Elementarzelle.
und dem Gitterparameter a = 302,4 pm sowie zwei Formeleinheiten pro Elementarzelle.